셀트리온(대표이사 기우성 김형기 서진석)이 자가면역 질환 치료제 '앱토즈마'를 미국 시장에 공식 출시했다. 오리지널 대비 35% 낮춘 약가 전략과 보험사 처방집 등재를 통해 조기 시장 안착을 추진한다.
셀트리온은 이달 초 미국 시장에 자가면역질환 치료제 ‘앱토즈마’(성분명: 토실리주맙)를 출시했다고 13일 밝혔다.
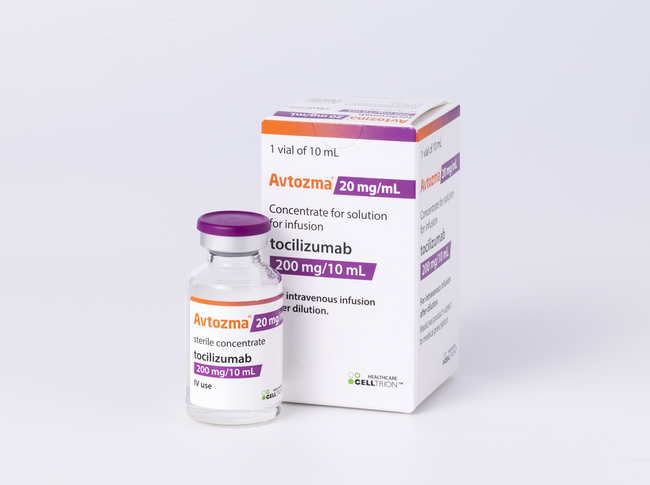 셀트리온의 앱토즈마 IV 제형 사진. [이미지=셀트리온]이번 출시 제품은 정맥주사(IV) 제형으로 셀트리온이 직접 판매망을 운영한다. 앱토즈마는 오리지널 의약품(로슈 ‘악템라’) 대비 약 35% 인하된 도매가격(High WAC)으로 출시돼, 경쟁력과 수익성을 동시에 확보할 수 있도록 설계됐다.
셀트리온의 앱토즈마 IV 제형 사진. [이미지=셀트리온]이번 출시 제품은 정맥주사(IV) 제형으로 셀트리온이 직접 판매망을 운영한다. 앱토즈마는 오리지널 의약품(로슈 ‘악템라’) 대비 약 35% 인하된 도매가격(High WAC)으로 출시돼, 경쟁력과 수익성을 동시에 확보할 수 있도록 설계됐다.
앱토즈마는 인터루킨(IL)-6 단백질 억제를 통해 염증 반응을 줄이는 기전의 인터루킨 억제제로 지난 1월 미국 FDA로부터 앱토즈마의 정맥주사(IV)와 피하주사(SC) 제형에 대한 품목 허가를 획득했다. 적응증은 류마티스관절염(RA), 거대세포동맥염(GCA), 소아특발성관절염(sJIA, pJIA), 코로나19 및 사이토카인방출증후군(CRS) 등이다. 특히 오리지널과 동일한 전체 적응증(Full Label)을 획득했다.
앱토즈마는 출시 직후 미국 대형 보험사인 블루크로스 블루쉴드(BCBS) 미네소타주 처방집에 선호의약품(Preferred Drug)으로 등재됐다. BCBS는 미국 전역에서 주별로 운영되는 건강보험 연합체로, 1억 명 이상의 가입자를 보유하고 있다.
이어 셀트리온은 현재 미국 3대 처방약급여관리업체(PBM) 를 포함한 주요 보험사와의 협상을 이어가고 있다. 업계에서는 BCBS 등재를 계기로 추가 보험사 확산이 가속화될 것으로 보고 있다.
더불어 앱토즈마의 핵심 적응증인 류마티스관절염(RA) 분야에서 처방 확대를 위해 전문 인력을 보강하고 있다. 또 피하주사(SC) 제형의 출시도 준비 중으로, 환자 상태에 따른 맞춤형 치료를 강화할 계획이다.
토마스 누스비켈(Thomas Nusbickel) 미국 법인 최고상업책임자(CCO)는 “셀트리온이 구축한 네트워크와 마케팅 역량을 기반으로 앱토즈마의 시장 안착 속도를 높일 것”이라며 “합리적인 가격으로 고품질 바이오의약품을 제공해 미국 의료현장의 신뢰를 강화하겠다”고 밝혔다.
